suivant: Définition cinétique de la
monter: Théorie cinétique des gaz
précédent: Modèle du gaz parfait
Table des matières
Index
Si l'on considère un gaz parfait dans un récipient, il faut comprendre que la notion de pression exercée par le gaz sur une paroi du récipient est liée à la présence même de ladite paroi.
La pression du gaz se définit ainsi comme la force moyenne par unité de surface exercée par le gaz sur les parois du récipient. Par suite, on peut déterminer l'expression de cette pression cinétique :
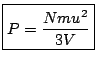 |
(1.5) |
où
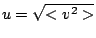 est la vitesse quadratique moyenne des particules de gaz parfait,
est la vitesse quadratique moyenne des particules de gaz parfait,  le nombre de molécules contenues dans le volume
le nombre de molécules contenues dans le volume  de gaz parfait. En fait, la distribution de vitesses des molécules est une distribution de Maxwell, les valeurs moyennes des trois composantes de la vitesse sont nulles et ainsi
de gaz parfait. En fait, la distribution de vitesses des molécules est une distribution de Maxwell, les valeurs moyennes des trois composantes de la vitesse sont nulles et ainsi
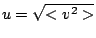 .
.





suivant: Définition cinétique de la
monter: Théorie cinétique des gaz
précédent: Modèle du gaz parfait
Table des matières
Index
Clément Baruteau
2003-04-30