




suivant: Diagramme d'équilibre (P,T)
monter: Changements d'état d'un corps
précédent: Changements d'état d'un corps
Table des matières
Index
Un corps pur, dont la composition chimique est bien définie, peut exister sous trois phases différentes : solide, liquide et vapeur. L'évolution d'une phase à une autre est appelée changement d'état, elle peut être exothermique si l'état final a une énergie plus faible que l'état initial, ou endothermique dans le cas contraire.
On définit la variance comme le nombre de paramètres d'état intensifs nécessaire et suffisant pour définir un état d'équilibre d'un système. La relation entre la phase  et la variance
et la variance  d'un système est donnée par la règle des phases de Gibbs:
d'un système est donnée par la règle des phases de Gibbs:
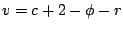 |
(1.44) |
où 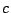 est le nombre de constituants mis en jeu par la ou les réactions et
est le nombre de constituants mis en jeu par la ou les réactions et  le nombre de réactions (attention: une réaction réversible compte pour une seule réaction).
On peut l'illustrer sur l'exemple suivant: considérons de l'étain fondu dans un creuset et étudions son refroidissement au cours du temps (figure (1.6), page
le nombre de réactions (attention: une réaction réversible compte pour une seule réaction).
On peut l'illustrer sur l'exemple suivant: considérons de l'étain fondu dans un creuset et étudions son refroidissement au cours du temps (figure (1.6), page ![[*]](file:/usr/lib/latex2html/icons/crossref.png) ). Nous observons que:
). Nous observons que:
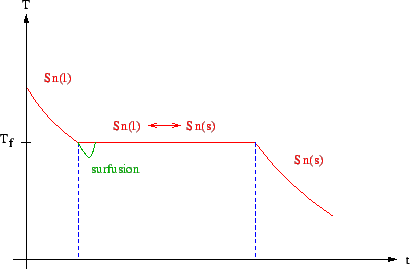
Figure 1.6:
Evolution avec le temps du refroidissement d'un bloc d'étain dans un creuset: illustration de la règle des phases de Gibbs.
|
|
- -
- Lorsque l'étain est sous une seule phase (liquide ou solide), la température diminue donc varie indépendamment de la pression qui reste constante. Pour définir l'état de ce système sous une seule phase, deux paramètres d'état intensifs sont ainsi nécessaires (
 et
et  dans de cas).
dans de cas).
- -
- Lorsque l'étain se retrouve sous deux phases (ici lors de l'équilibre des phases liquide et gazeuse), la température comme la pression restent cons-tantes. Il existe donc une relation entre température et pression à l'équilibre, et un seul paramètre d'état intensif est donc nécessaire pour décrire l'état de notre système quand il est diphasé.
La relation (1.45) est valable dans le cadre de la thermochimie de deuxième année; pour la première année, on se contentera de l'égalité
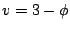 qui conforte les observations faites dans l'exemple ci-dessus; ainsi, un système:
qui conforte les observations faites dans l'exemple ci-dessus; ainsi, un système:
- -
- monophasé est divarient.
- -
- diphasé est monovariant.
- -
- triphasé est zéro variant (c'est l'exemple du point triple de l'eau).





suivant: Diagramme d'équilibre (P,T)
monter: Changements d'état d'un corps
précédent: Changements d'état d'un corps
Table des matières
Index
Clément Baruteau
2003-04-30
![]() et la variance
et la variance ![]() d'un système est donnée par la règle des phases de Gibbs:
d'un système est donnée par la règle des phases de Gibbs:
![]() qui conforte les observations faites dans l'exemple ci-dessus; ainsi, un système:
qui conforte les observations faites dans l'exemple ci-dessus; ainsi, un système: